告别小鼠模型?革命性“人源类器官”平台问世!Nat Commun:科学家造出“人体活试纸”,一次性筛选近两千个癌症靶点
时间:2025-08-21
告别小鼠模型?革命性“人源类器官”平台问世!Nat Commun:科学家造出“人体活试纸”,一次性筛选近两千个癌症靶点
来源:100医药网 2025-08-21 10:25
本研究在人类3D胃类器官中进行大规模CRISPR筛选,发现岩藻糖基化和TAF6L调控顺铂敏感性,揭示基因-药物相互作用机制,凸显类器官在癌症研究中的价值。
在癌症治疗中,相同的药物对不同患者往往效果迥异,这种个体差异背后,基因与药物的相互作用扮演着关键角色。然而,要在贴近人体生理环境的系统中解析这些相互作用并非易事。
近日,Nat Commun发表的一项研究Large-scale CRISPR screening in primary human 3D gastric organoids enables comprehensive dissection of gene-drug interactions为解决这一难题带来了新突破,研究团队借助大规模CRISPR基因编辑技术,在原发性人类3D胃类器官中成功开展了基因-药物相互作用的系统分析,揭示了影响顺铂敏感性的关键基因和机制。

人类3D类器官作为一种新兴模型,能很好地保留原发组织的结构、活性、分化特性及基因组特征,在癌症生物学研究和医疗中展现出巨大潜力。但此前,由于缺乏高通量功能分析的基因组编辑工具,利用类器官全面解析基因-药物相互作用一直受限。而CRISPR技术的发展为基因组编辑提供了精准高效的工具,此次研究将其与3D胃类器官结合,实现了包括基因敲除、干扰(CRISPRi)、激活(CRISPRa)及单细胞分析在内的大规模筛选。
研究首先构建了稳定表达Cas9的TP53/APC双敲除(DKO)胃肿瘤类器官模型,该模型遗传背景相对均一,有助于精准识别基因功能关系。通过验证实验,证实了CRISPR/Cas9在类器官中具有高效切割活性,95%以上的Cas9表达细胞能成功敲除GFP报告基因。随后的试点筛选使用包含12461个sgRNA的文库,靶向1093个膜蛋白基因,发现了68个显著影响细胞生长的基因,这些基因富集于转录、RNA加工等关键生物学过程,且部分基因经独立验证确认了其对生长的调控作用。
为实现基因表达的时空调控,研究建立了多西环素诱导的CRISPRi和CRISPRa系统。该系统能有效下调或上调靶基因表达,如对CXCR4和SOX2的调控效果显著。基于此,团队设计了针对1952个DNA和RNA结合蛋白基因的sgRNA文库,在有无顺铂处理的类器官中进行筛选。结果显示,CRISPRi筛选发现41个顺铂敏感基因和9个缓冲基因,涉及核苷酸切除修复(NER)、同源重组修复(HRR)等通路;CRISPRa筛选则发现9个过表达可增强顺铂敏感性的基因。其中,NER通路的ERCC6、ERCC4,HRR通路的BRCA1等已知基因的发现验证了筛选系统的可靠性,同时还识别出ELOF1、LEO1等新候选基因。
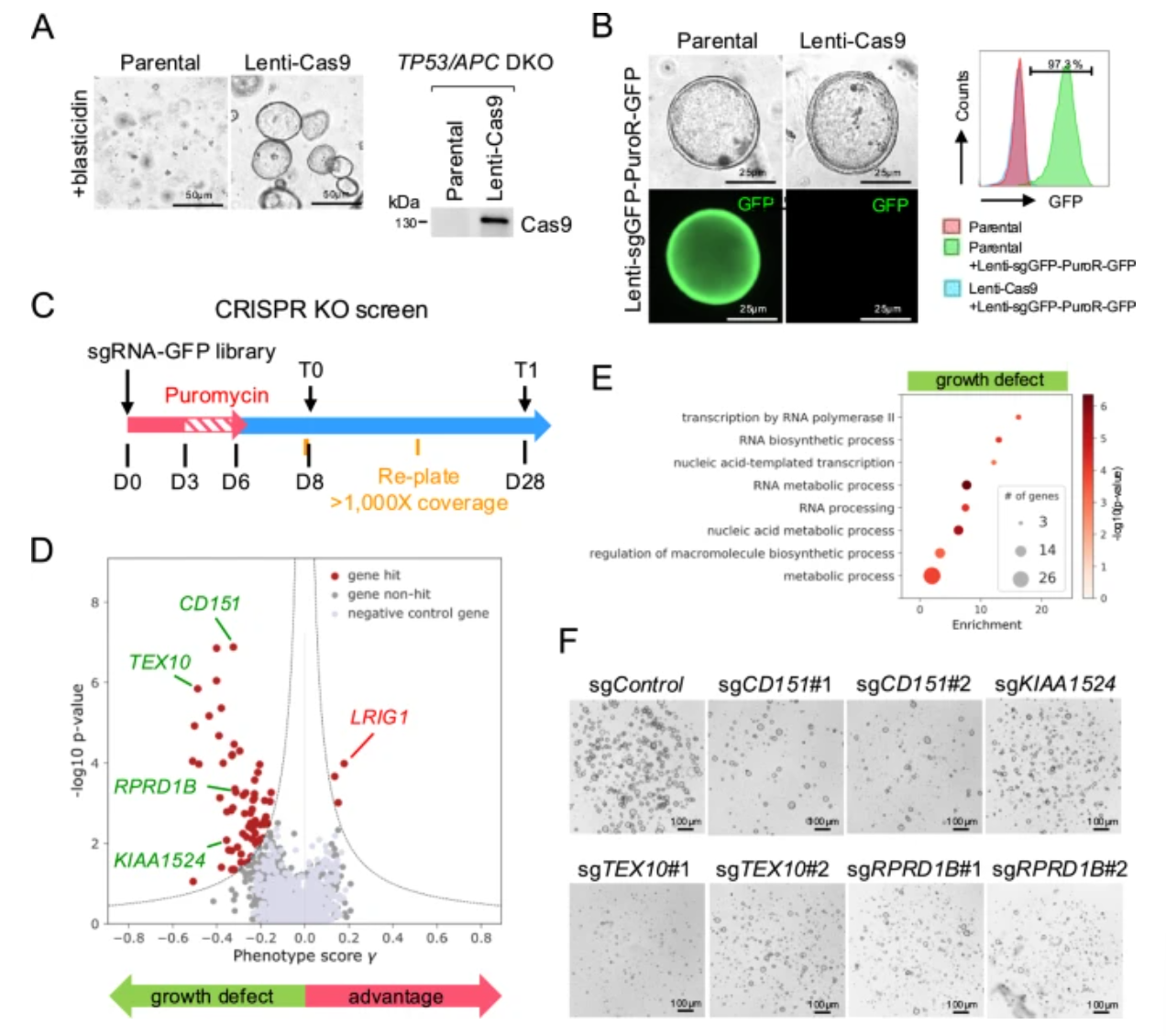
图1 CRISPR KO筛选在TP53/APC双敲除致癌基因工程化人胃类器官中的应用
单细胞CRISPR筛选进一步揭示了基因-药物相互作用的深度机制。在顺铂处理下,原本转录组存在差异的NER和HRR通路基因敲除细胞,呈现出趋同的转录特征,分别聚类成不同群体。更令人意外的是,研究发现顺铂与NER基因敲除结合会协同抑制GMDS 一种参与GDP-岩藻糖合成的关键酶,导致细胞整体岩藻糖基化水平降低。而GMDS过表达会增强顺铂敏感性,抑制岩藻糖基化则降低敏感性,表明岩藻糖基化下调可能是细胞应对顺铂损伤的一种保护性机制。
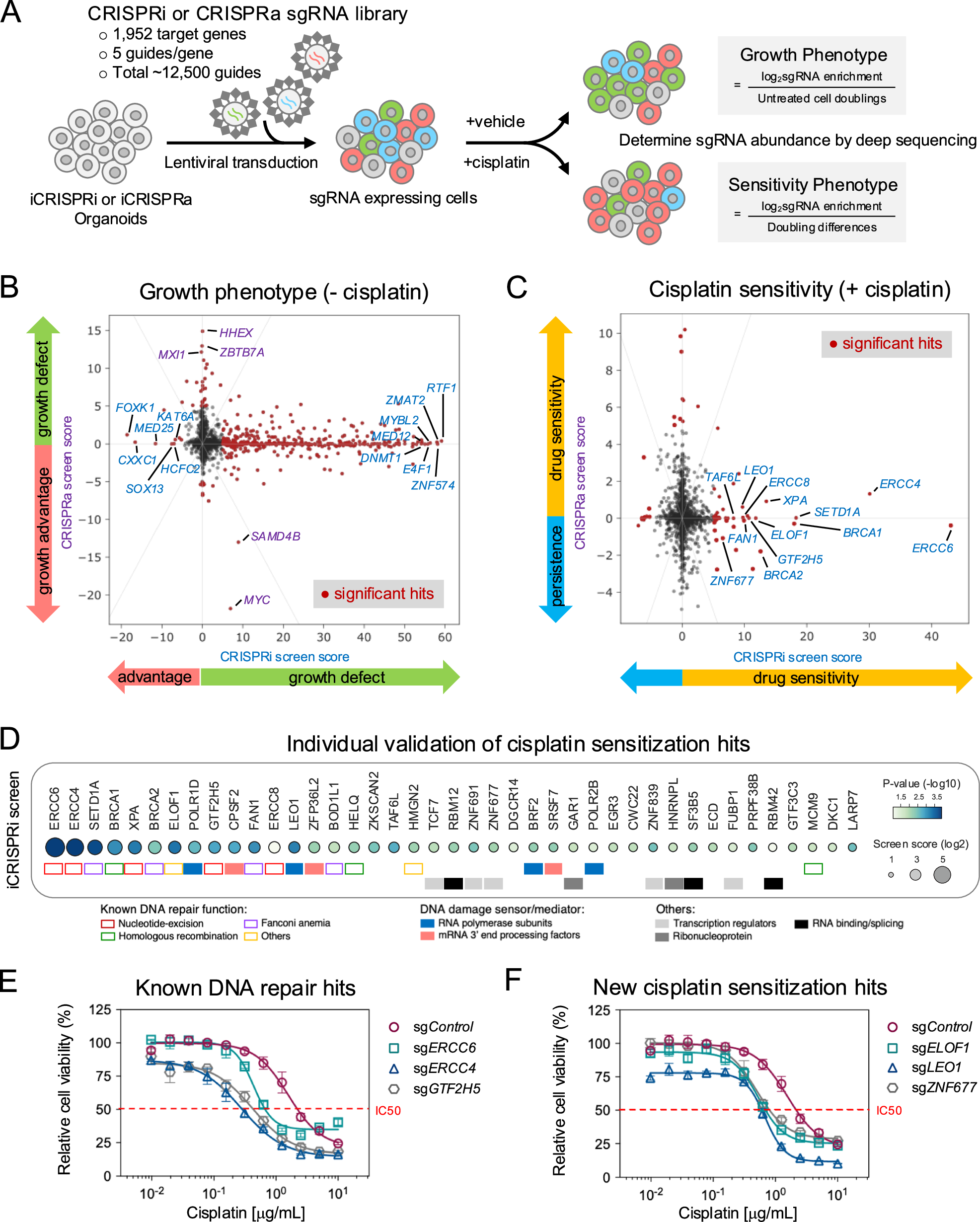
图2 人类类器官中的大规模iCRISPRi和iCRISPRa筛选揭示基因-药物依赖性
此外,研究还发现TAF6L是顺铂敏感性的关键调控因子。TAF6L敲除会增强类器官对顺铂的敏感性,而过表达则起到保护作用。机制上,TAF6L并非直接参与DNA修复,而是通过维持细胞在顺铂损伤后的增殖能力,促进细胞恢复。ATAC-seq分析显示,TAF6L敲除会导致染色质可及性显著降低,提示其可能通过调控基因组区域的可及性影响细胞增殖相关基因的表达。
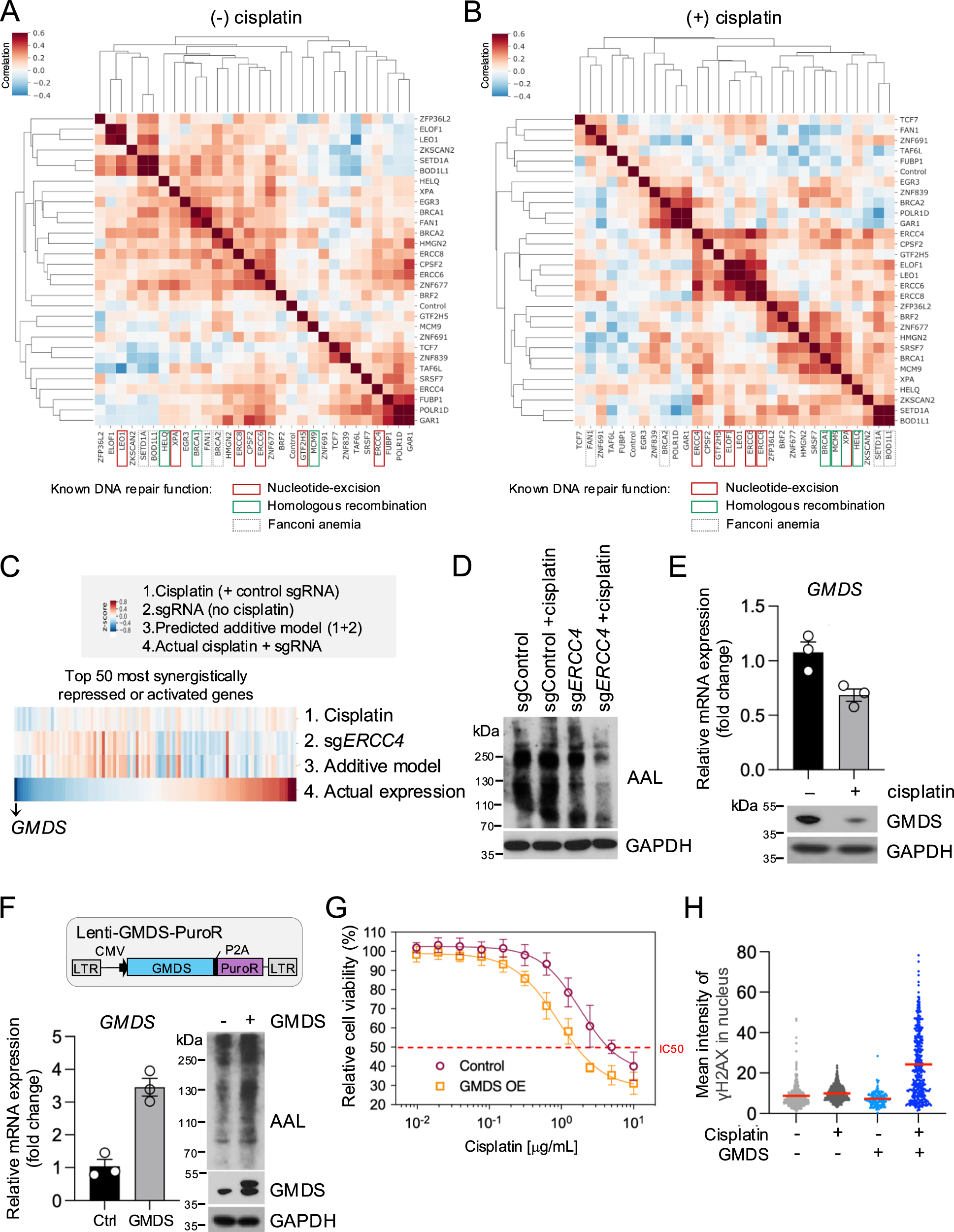
图3 高维单细胞转录组揭示基因-药物相互作用的协同效应
这项研究充分展示了人类类器官模型在解析基因-药物相互作用中的独特价值,不仅鉴定出影响顺铂敏感性的新基因和通路,如岩藻糖基化与DNA修复的跨界关联、TAF6L在细胞损伤恢复中的作用,更为个性化癌症治疗提供了潜在的治疗靶点和研究思路。未来,类似的研究方法有望扩展到更多物和其他类型的类器官模型,推动癌症基础研究和临床转化的双重突破,为癌症患者带来更精准有效的治疗方案。(100yiyao.com)
参考文献:
Lo YH, Horn HT, Huang MF, et al. Large-scale CRISPR screening in primary human 3D gastric organoids enables comprehensive dissection of gene-drug interactions.Nat Commun. 2025;16(1):7566. Published 2025 Aug 14. doi:10.1038/s41467-025-62818-3
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载->
