信立泰发力 一类新药抢攻250亿市场
时间:2022-11-25
11月22日,信立泰发布公告称,公司自主研发的创新小分子药物SAL0119临床试验申请获得受理。目前拟开发的临床适应症包括活动期强直性脊柱炎和中重度活动期类风湿性关节炎。截至目前,信立泰今年已经申请了4个一类新药。
图1:信立泰申报的最新产品
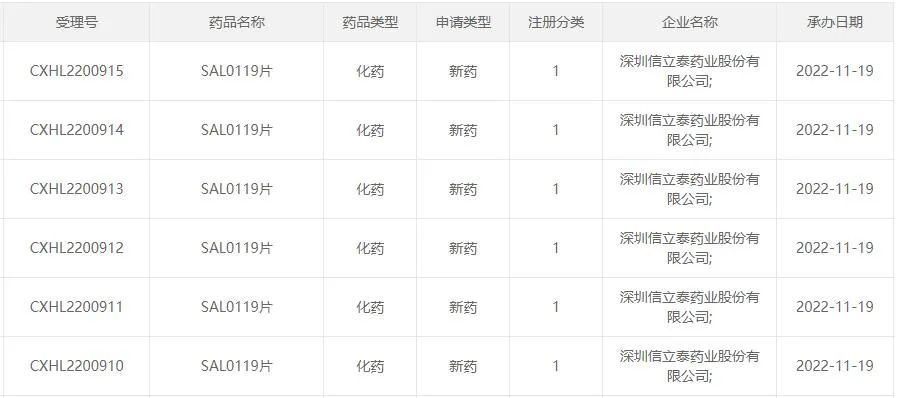
来源:CDE官网
欣泰在公告中提到,SAL0119片为口服小分子免疫抑制剂。目前要开发的临床适应症包括活动期强直性脊柱炎和中重度活动期类风湿性关节炎。强直性脊柱炎(AS)和类风湿性关节炎(RA)都是自身免疫性疾病。目前,该病的病因还不完全清楚,也没有治愈的方法。SAL0119具有不同于JAK的独特作用机制和广谱细胞因子抑制作用。临床前研究数据显示了良好的有效性和安全性。
图2:国内免疫抑制剂销售额(单位:万元)

来源:内部网模式数据库
近年来,随着越来越多的新产品获准进入市场,免疫抑制剂的整体销售规模迅速增长。根据Minenet的数据,2021年免疫抑制剂在三大终端、六大市场(统计范围见文末)的销售总额已经超过250亿元。公立医院终端(城市公立医院中的县级公立医院)是主战场,占比超过80%,零售药店终端(城市实体药店中的网上药店)在最近两年快速增长。
图3:信立泰今年申报的一类新药情况。
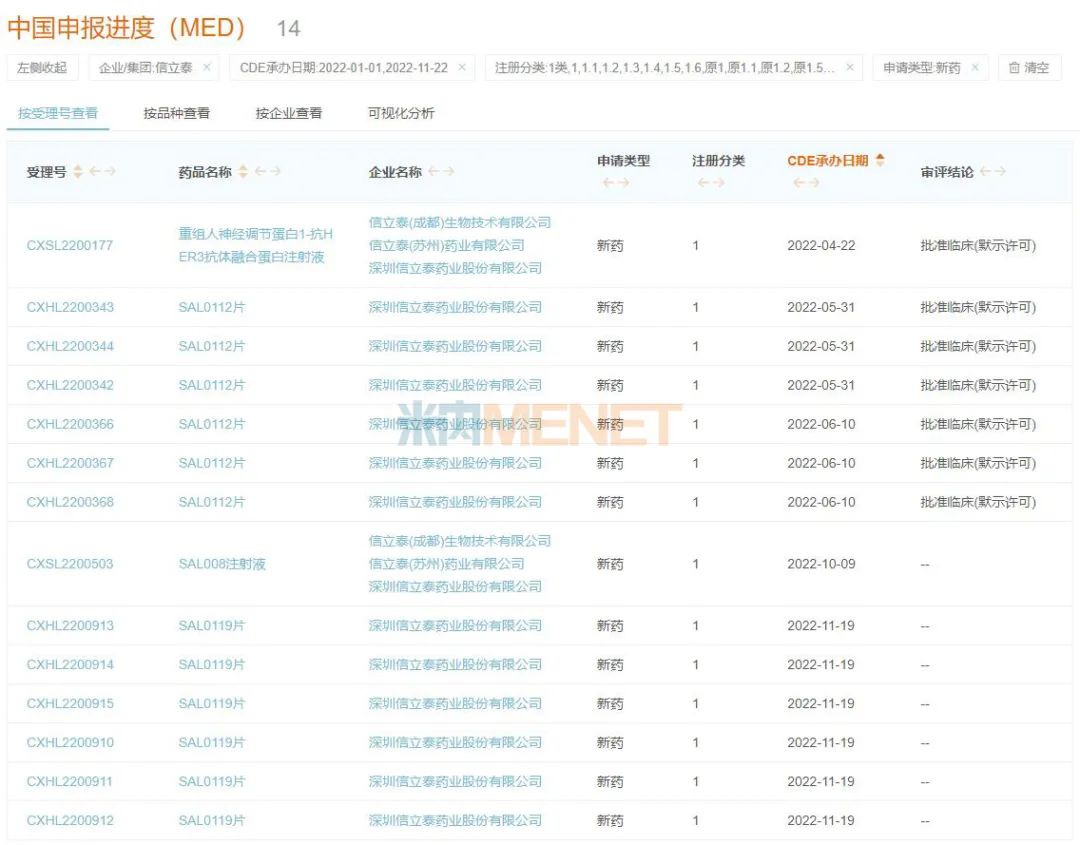
来源:Minenet新数据库
截至目前,信立泰今年已申报4个1类新药,其中重组人神经调节蛋白1-抗HER3抗体融合蛋白注射液和SAL0112片已获得临床批准。
据悉,重组人神经调节蛋白1-抗HER3抗体融合蛋白注射液是信立泰在中国和美国报道的首个创新型生物制药。目前,HFrEF(射血分数保留的心力衰竭)的适应症正在中国和美国进行I期临床研究。
SAL0112片剂是一种口服GLP-1R小分子偏向激动剂,其用于体重管理的适应症包括二型糖尿病、成人肥胖患者或超重患者,已获得临床批准。
SAL008注射液是IL-15/IL-15R复合物和抗CTLA-4抗体的融合蛋白,用于治疗晚期实体肿瘤。目前我国新药临床应用正在审评审批中。新药在欧洲提交CTA(欧洲临床试验申请)后,已经开始I期临床研究。
来源:CDE官方网站、公司公告和内网数据库。
注:Minenet 《中国三大终端6大市场药品竞争格局》,统计范围为:城市公立医院和县级公立医院、城市社区中心和乡镇卫生院、城市实体药店和网上药店,不包括民营医院、私人诊所、村卫生室和县乡药店;以上销售额是根据产品在终端的平均零售价格计算的。统计截至11月23日,如有遗漏,敬请指正!
