Nat Commun:胎盘衍生因子促进人iPSC肝脏类器官生长
时间:2025-04-06
技术流程图:
hiPSC 三系分化 类器官球体 缺氧 + IL1 刺激 3D 功能检测 机制解析
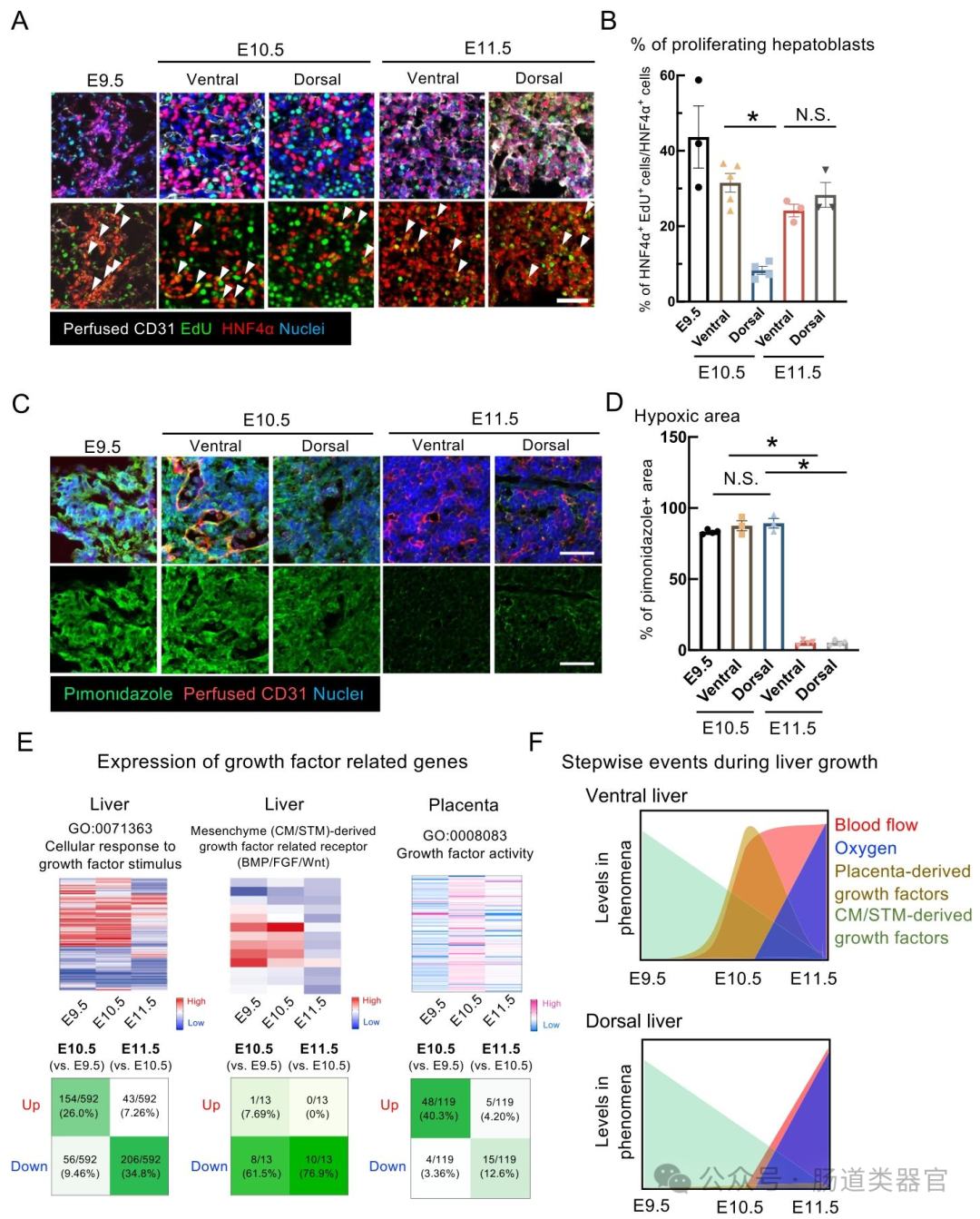
研究团队针对人诱导多能干细胞(hiPSC)肝脏类器官因祖细胞扩增不足导致的尺寸与功能限制问题,提出胎盘衍生因子在特定时空微环境中调控祖细胞扩张的科学假说。研究通过三维成像技术发现,小鼠胚胎肝在E10.5阶段经历短暂缺氧期(图1D),此时胎盘特异性分泌IL1 (图3G)。为验证这一机制,研究采用体内外联合实验:在胎肝离体培养中,添加IL1 使肝实质面积增加2.3倍(图3F);在hiPSC类器官中,缺氧条件下IL1 处理7天可使HNF4 ⁺区域体积增大4.8倍(图4B)。机制研究显示,IL1 通过激活间充质细胞的SAA1-TLR2-CCL20-CCR6通路(图4K),促进肝祖细胞增殖。值得注意的是,序贯氧合处理进一步提升类器官功能,ALB分泌量较对照组增加3.2倍(图5D)。该研究首次揭示胎盘-肝脏互作的关键调控因子,并建立"缺氧预处理+胎盘因子刺激"的新型培养策略,为功能性类器官构建提供范式。然而,胎盘因子的时空特异性递送机制、多因子协同效应以及长期培养中的代谢调控仍需深入探索。未来可结合微流控芯片技术(图5A),模拟胎儿血流环境,系统解析胎盘因子与机械应力的动态互作。