Nature:李子海团队揭开T细胞耗竭的根本机制——蛋白错误折叠引起的毒性应激反应,为新一代癌症免疫疗法指明方向
时间:2025-10-04
Nature:李子海团队揭开T细胞耗竭的根本机制——蛋白错误折叠引起的毒性应激反应,为新一代癌症免疫疗法指明方向
来源:生物世界 2025-10-04 10:05
该研究首次发现,大量错误折叠蛋白质堆积引发的非经典蛋白毒性应激反应(PSR)是驱动 T 细胞耗竭和免疫逃逸的关键机制,研究团队将其命名为为 Tex-PSR(T 细胞耗竭特异性蛋白质毒性应激反应)。T 细胞耗竭(T cell exhaustion)是一种功能减退状态,其特征为效应功能减弱以及抑制性受体表达增加,这种状态由持续的抗原暴露和不利的微环境所导致。在癌症中观察到耗竭T 细胞(Tex)无法清除恶性细胞,这也是癌症患者对疗法产生抗性的关键机制。
该耗竭程序产生异质性的 Tex 细胞群,其中祖细胞耗竭 T 细胞(Tprog)细胞保留了干性和自我更新能力,能够对免疫检查点阻断(ICB)疗法作出响应,并分化为具有细胞溶解能力的中间耗竭 T 细胞(Tint)。相反,终末耗竭 T 细胞(Ttex)细胞会随着时间的推移而累积,并且对免疫检查点阻断疗法响应不佳。
此外,T 细胞耗竭还限制了 细胞疗法对实体瘤的治疗效果。因此,更好地理解 T 细胞耗竭,对于克服当前癌症免疫疗法的局限性至关重要。
2025 年 10 月 1 日,俄亥俄州立大学李子海教授团队(王怡为第一作者)在国际顶尖学术期刊Nature上发表了题为:Proteotoxic stress response drives T cell exhaustion and immune evasion的研究论文。
该研究首次发现,大量错误折叠蛋白质堆积引发的非经典蛋白毒性应激反应(Proteotoxic Stress Response,PSR)是驱动T 细胞耗竭和免疫逃逸的关键机制,研究团队将其命名为为Tex-PSR(T 细胞耗竭特异性蛋白质毒性应激反应)。
这项研究将我们对 T 细胞耗竭的理解从转录组学层面深入到了蛋白质组学和细胞稳态层面,表明了靶向蛋白质稳态通路可作为癌症免疫治疗的一个新方向。
尽管转录组学分析为 T 细胞耗竭(Tex)细胞生物学提供了见解,但在不同生物体中,mRNA 丰度并不总是蛋白质表达水平的可靠替代指标。之前的研究表明,无论功能状态如何,T 细胞中 mRNA 与蛋白质的相关性都很差,并且转录后调控在 T 细胞分化和功能中具有重要意义。在此背景下,绘制 Tex 细胞的高分辨率蛋白质组图谱将很有价值。
在这项最新研究中,研究团队定义了不同条件下 Tex 细胞的蛋白质组全景图谱,包括体外耗竭模型、小鼠体内慢性淋巴细胞性脉络丛脑膜炎病毒(LCMV)感染以及结肠肿瘤和膀胱肿瘤小鼠模型。研究团队证明了,在特定通路中,mRNA 转录水平和蛋白质水平之间存在不一致。
该研究进一步定义了一种名为 Tex-PSR 的独特细胞反应,即T 细胞耗竭特异性蛋白质毒性应激反应。这是一种发生在耗竭 T 细胞(Tex)内部的应激反应,源于细胞内产生了大量错误折叠或受损的蛋白质,导致了 蛋白质毒性 (Proteotoxicity)。
Tex-PSR的主要特征包括
整体蛋白质合成增加:与经典的未折叠蛋白反应(UPR)通常会抑制蛋白合成以减轻应激压力不同,Tex-PSR 的一个显著特征是全局蛋白合成速率异常升高;
特异性分子伴侣激活:细胞试图应对这些错误折叠的蛋白质,于是选择性地上调了分子伴侣蛋白(特别是gp96和BiP)。这些伴侣蛋白努力帮助蛋白质正确折叠,但显然无法应对;
蛋白质聚集体积累:尽管有伴侣蛋白的帮助,过多的错误折叠蛋白仍然超出了细胞的清理能力,导致细胞内形成不溶性的蛋白质聚集体,这会进一步破坏细胞功能。
由持续 AKT 信号驱动:这一系列事件的核心驱动因素是AKT 信号通路的持续激活。AKT 是促进细胞生长、增殖和代谢的关键通路,它的过度活跃可能导致了蛋白合成的 失控 。
研究团队进一步发现,仅通过向正常的效应 T 细胞(Teff)中引入错误折叠的蛋白质,就足以直接诱导它们转变为耗竭 T 细胞(Tex)。这证明了蛋白质毒性应激反应(PSR)与 T 细胞耗竭之间不仅仅是相关性,而是因果关系 蛋白质稳态的失调本身就是导致 T 细胞耗竭的一个根本原因。
该研究还发现,这种 Tex-PSR 特征同样存在于人类癌症患者的耗竭 T 细胞(Tex)中,且与临床免疫治疗响应不良有关,证明了该发现具有重要的临床应用价值。
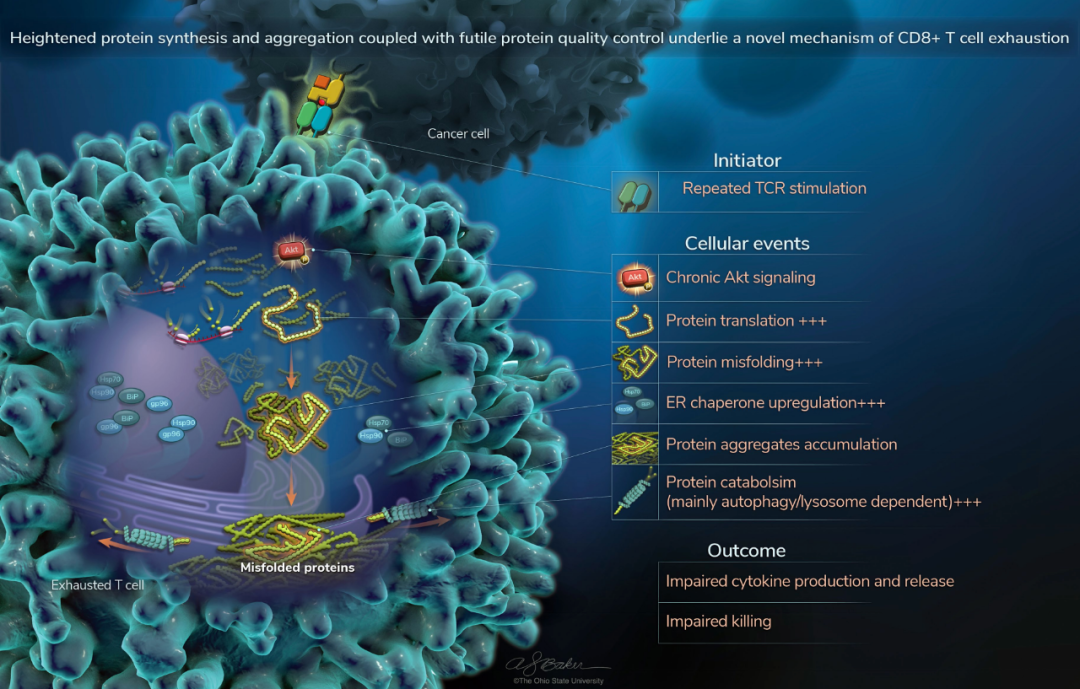
Tex-PSR 作为 CD8+ T 细胞耗竭的机制驱动因素
这项研究为开发下一代免疫疗法开辟了全新方向 除了靶向细胞表面的 PD-1/PD-L1,或许还可以靶向细胞内部的 Tex-PSR 通路(例如,抑制 AKT、调控分子伴侣、清除蛋白聚集体),从而从根本上恢复 T 细胞活力,逆转耗竭,提高癌症免疫治疗的疗效。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载->
